 Ảnh 1: Gốc axit có thể tìm thấy nhiều ở môi trường xung quanh chúng ta
Ảnh 1: Gốc axit có thể tìm thấy nhiều ở môi trường xung quanh chúng ta
Gốc axit là thuật ngữ quen thuộc trong lĩnh vực hóa học và nghiên cứu về sức khỏe. Để hiểu rõ và áp dụng tốt kiến thức về axit, cùng tìm hiểu chi tiết về gốc axit và ứng dụng của chúng.
1. Gốc axit là gì?
Axit là một phân tử hóa học được cấu tạo bởi nguyên tử Hydro và gốc axit. Để có được gốc axit, chỉ cần tách nguyên tử Hydro ra khỏi phân tử hóa học. Gốc axit có thể được tìm thấy trong nhiều môi trường xung quanh chúng ta, bao gồm cả thực vật và thực phẩm hàng ngày như hoa quả có vị chua, chanh. Ngay cả nguồn nước mà chúng ta sử dụng hàng ngày, nếu không được lọc sạch, cũng có thể chứa gốc axit. Đồ uống chứa axit như bia, rượu, đồ uống có ga, cồn và thực phẩm giàu chất béo cũng chứa gốc axit.
 Hình 2: Phân loại các gốc axit dựa vào đặc tính của chúng
Hình 2: Phân loại các gốc axit dựa vào đặc tính của chúng
2. Phân loại gốc axit gồm những gì?
Gốc axit có thể được chia thành hai loại dựa trên cấu trúc: gốc axit có hydro và gốc axit không có hydro.
2.1. Gốc axit có hydro
Các gốc axit có hydro bao gồm: -HSO4, =HPO4, -H2PO4.
2.2. Gốc axit không có hydro
Các gốc axit không có hydro bao gồm: -Cl, -NO3, =SO4, PO4.
Ngoài ra, axit cũng được phân loại thành axit có oxy và axit không có oxy. Các gốc axit có oxy bao gồm: -NO3, =SO4, PO4. Các gốc axit không chứa oxy bao gồm: -Cl, -Br, -F, -I.
3. Tính chất hóa học của axit
Cùng tìm hiểu về một số tính chất hóa học của axit để hiểu thêm về gốc axit.
3.1. Axit làm đổi màu giấy quỳ tím
Khi đổ một vài giọt dung dịch axit vào giấy quỳ tím, màu của giấy sẽ chuyển sang màu đỏ. Điều này cho thấy dung dịch axit làm đổi màu giấy quỳ tím thành đỏ. Giấy quỳ tím được sử dụng để nhận biết dung dịch axit.
3.2. Axit tác dụng với kim loại
Khi axit tác dụng với các kim loại, ta sẽ nhận được một muối và khí hidro. Phản ứng này chỉ xảy ra với các kim loại đứng trước nguyên tử Hydro trong dãy hoạt động hóa học.
3.3. Tác dụng với bazơ
Khi axit tác dụng với bazơ, phản ứng mãnh liệt xảy ra và ta sẽ nhận được một muối và nước. Đây được gọi là phản ứng trung hòa.
3.4. Tác dụng với oxit bazơ
Tất cả các axit đều tác dụng với oxit bazơ và tạo thành muối và nước.
3.5. Tác dụng với muối
Axit tác dụng với muối tạo ra các trường hợp sau:
- Chất tạo thành có kết tủa hoặc khí bay hơi.
- Nếu muối mới là muối tan, axit mới là axit yếu. Nếu muối mới là muối không tan, axit mới là axit mạnh.
4. Ứng dụng của một số axit
Axit có nhiều ứng dụng trong các lĩnh vực khác nhau, bao gồm công nghiệp, công nghệ thực phẩm, y tế và cơ thể người.
4.1. Lĩnh vực công nghiệp
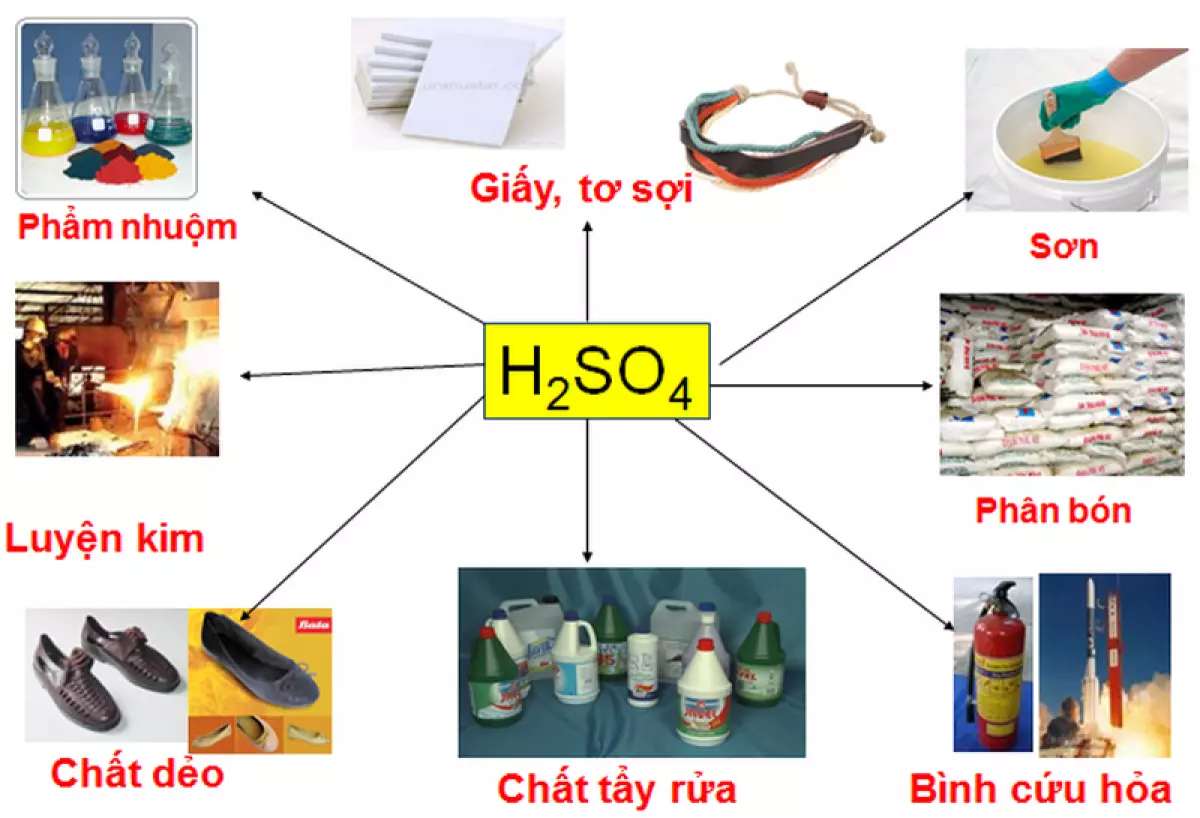
Axit được sử dụng trong việc loại bỏ gỉ sắt, làm sạch bề mặt trước khi hàn, sử dụng trong pin xe hơi, bình acquy; sản xuất phân bón, tẩy rửa, dầu mỏ, muối, axit, thuốc nổ, luyện kim, chất dẻo, tẩy trắng giấy,...
4.2. Công nghệ thực phẩm
Axit được sử dụng trong chất tạo màu, điều chỉnh độ chua, chất chống tạo bọt, chất chống vón, chất chống oxy hóa, chất tạo lượng, giữ màu, chất chuyển thể sữa, tạo vị, xử lý bột ngũ cốc, giữ ẩm, chất ổn định,...
4.3. Lĩnh vực y tế
Axit được sử dụng trong sản xuất thuốc, chẳng hạn như Aspirin, một loại thuốc giảm sốt được nghiên cứu từ cuối thế kỷ 19.
4.4. Trong cơ thể người
Axit đóng vai trò quan trọng trong tiêu hóa thức ăn, tổng hợp protein, sản xuất DNA và RNA, duy trì độ cân bằng pH trong cơ thể.
Hy vọng rằng bạn đã hiểu thêm về gốc axit và các tính chất của chúng. Gốc axit được ứng dụng rất nhiều trong đời sống và công nghiệp để bảo quản thực phẩm và tạo ra các sản phẩm hữu ích.

















